SET8诱导UHRF1和DNMT1降解、防止DNA过度甲基化
SET8诱导UHRF1和DNMT1降解、防止DNA过度甲基化01 文章背景简介泛素化是指泛素(一类低分子量的蛋白质)分子在一系列特殊的酶作用下,将细胞内的蛋白质分类,从中选出靶蛋白
01 文章背景简介
泛素化是指泛素(一类低分子量的蛋白质)分子在一系列特殊的酶作用下,将细胞内的蛋白质分类,从中选出靶蛋白分子,并对靶蛋白进行特异性修饰的过程。这些特殊的酶包括泛素激活酶、结合酶、连结酶和降解酶等。同时,它也参与了细胞周期、增殖、凋亡、分化、转移、基因表达、转录调节、信号传递、损伤修复、炎症免疫等几乎一切生命活动的调控。
在哺乳动物中,DNA甲基化主要发生在CpG二核苷酸环境中的胞嘧啶-C5位点,在转录调控、异染色质形成、X染色体失活、印记和基因组稳定性等方面起关键作用。有三种活跃的DNA甲基转移酶——DNMT3A,DNMT3B和DNMT1协同作用以建立和维持给定细胞的DNA甲基化,DNMT1主要负责将在DNA复制过程中产生的半甲基化CpG底物转化为对称的甲基化分子,这一过程称为DNA维持甲基化。在DNA维持甲基化过程中,UHRF1(ubiquitin-like with phd and ring finger domains 1,泛素样含PHD和环指域蛋白1)起着至关重要的作用,UHRF1是一种多结构和功能性核蛋白。UHRF1在S期通过其结合半甲基化的能力加载到复制叉上CpGs(新复制DNA的产物)通过一个独特的SRA结构域和组蛋白H3尾巴与二甲基或三甲基化K9 (H3K9me2/3)或甲基化DNA连接酶1通过串联都铎结构域和PHD结构域的联合作用。复制叉相关的UHRF1反过来泛素化组蛋白H3。通过与UHRF1、PCNA和泛素化H3的组合相互作用,DNMT1被招募到复制叉中。然而,这一过程是如何调节的还不是很清楚。
以前的许多研究都集中在调节DNMT1的表达及其对DNA甲基化的活性。例如,DNMT1的稳定性和活性已显示受翻译后修饰的调控,包括磷酸化、乙酰化和甲基化以及通过RNA。然而,关于通过调节UHRF1来控制DNA甲基化的研究较少。在这方面,作为募集和激活DNMT1的因素,UHRF1可能是DNA甲基化调控的更敏感靶标。最近的研究已经确定,UHRF1是重编程幼稚胚胎干(ES)细胞和卵子发生过程中整个DNA甲基化的关键靶标。在体细胞中,已知S期UHRF1的高表达与细胞增殖有关,并且通常在癌细胞中被解除控制。然而,目前尚不清楚UHRF1在体细胞中是如何调控、确保在细胞分裂中DNA甲基化的忠实遗传的。
已知SET8(也称为PR-SET7、SETD8和KMT5A)可以催化组蛋白H4Lys20和包括p53在内的非组蛋白的单甲基化(33)。SET8蛋白的表达是通过细胞周期来调控的,它在G1/S期被蛋白酶体降解。因此,SET8在G2/M和G1中高表达。在哺乳动物细胞中,SET8的缺失导致染色质过早致密化、G2/M阻滞和DNA损伤修复缺陷。然而,尚不清楚SET8是否调节DNA甲基化。
Zhang H等人于2019年在《Nucleic Acids Res》杂志上(IF 11.147,生物1区)发表了题为“SET8 prevents excessive DNA methylation by methylation-mediated degradation of UHRF1 and DNMT1”的文章。在本研究中,作者发现SET8通过甲基化依赖的蛋白降解,以细胞周期依赖的方式调控UHRF1。此外,SET8还调节DNMT1。本文表明,SET8是DNA甲基化的关键调控因子,通过控制DNA维持甲基化的轴,尤其是UHRF1,来确保DNA甲基化的稳态。
02 所用到的主要方法
(1)蛋白质印迹分析
(2)定量实时PCR
(3)免疫染色
(4)免疫共沉淀
(5)荧光激活细胞分选(FACS)分析
(6)EdU染色法
03 文章主要内容摘要
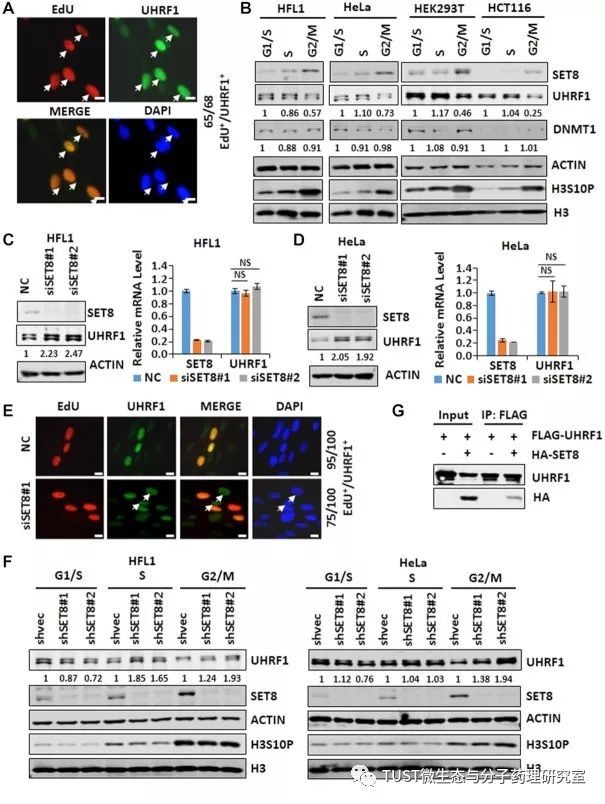
在细胞分裂过程中,DNA甲基化的忠实遗传需要DNMT1及其辅因子UHRF1。然而,这个轴是如何调控,以确保DNA甲基化稳态仍然知之甚少。本文发现:SET8是一种细胞周期调节的蛋白质甲基转移酶,它通过甲基化介导的泛素依赖降解来控制UHRF1和DNMT1的蛋白质稳定性,从而阻止DNA的过度甲基化。SET8在赖氨酸385处将UHRF1甲基化,这种修饰导致UHRF1的泛素化和降解。相反,LSD1通过去甲基化稳定UHRF1和DNMT1。因此,SET8和LSD1很可能通过调节UHRF1水平而不是DNMT1水平来调节整体DNA甲基化。最后,本文证明了SET8在G2/M中下调UHRF1,在抑制DNMT1介导的甲基化上有作用。总之,本研究揭示了SET8在促进DNA甲基化稳态中的新作用,并确定UHRF1是通过动态蛋白甲基化调节DNA甲基化。
-
SUV39H1/DNMT3A依赖的RB1启动子甲基化会刺激PIN1表达及黑色素瘤发展2019-10-25