君联医疗全球新药资讯速递 · 第19期
君联医疗全球新药资讯速递 · 第19期2019.8.19-2019.8.25,本周新药数据共10个,其中肿瘤4个,抗感染3个,心血管、基因疗法和皮肤各1个一周要点速览国家医疗保障局
2019.8.19-2019.8.25,本周新药数据共10个,其中肿瘤4个,抗感染3个,心血管、基因疗法和皮肤各1个
一周要点速览
国家医疗保障局发布2019版国家医保目录的常规目录部分,业内期待的医保目录调整终于开始落地。上一次医保目录公布是2017年,而再上一次就是遥远的2009年了,目录的迭代和evovle有加速的趋势。另外,本次目录调整的重大特色之一是小牛血、鼠神经生长因子等辅药被调出,这些神药当年几乎都可以凭借单药撑起一家上市公司。一代版本一代神,随着新目录的公布,属于辅药的黄金时代算是开始落幕了。后续医保局就创新药会产开一系列的谈判准入工作,应还会有一些重磅药物会成为幸运儿
阿斯列康宣布其SGLT2抑制剂Farxiga在心衰三期临床试验中达到一级终点,这是SGLT2抑制剂在前瞻性试验中首次显示心衰疗效。SGLT2此前由于降糖机制简单粗暴,在DM中一直被认为是偏房,所以AZ、礼来和强生都在寻找其他获益证据。礼来的Jardiance成为第一个显示心血管收益的降糖药物,从而弯道超车成为行业龙头。考虑到心衰存在巨大的unmet medical need,而且近20年没有新药,Farxiga这次奇兵突现,有可能会重构SGLT2的行业竞争格局
药品研发动态
GSK靶向BCMA的抗体偶联药物,在治疗复发/难治性MM患者
的关键性2期临床试验中获得积极结果
公司
GSK公司靶向B细胞成熟抗原(BCMA)的抗体偶联药物belantamab mafodotin,在治疗接受过多种前期疗法的复发/难治性多发性骨髓瘤(R/R MM)患者的关键性2期临床试验中获得积极结果
药物机理
belantamab mafodotin是将人源化抗BCMA抗体与细胞毒性剂连接在一起,通过靶向BCMA将细胞毒性剂特异性送入MM细胞中起到杀伤癌细胞的作用
入组标准与实验设计
2期,随机,开放标签的试验,共有196例R/R MM患者参与其中
结果
数据分析表明belantamab mafodotin能够达到60%的ORR,完全缓解率达到15%,无进展生存期(PFS)达到12个月
BCMA已经成为众多疗法的试验田
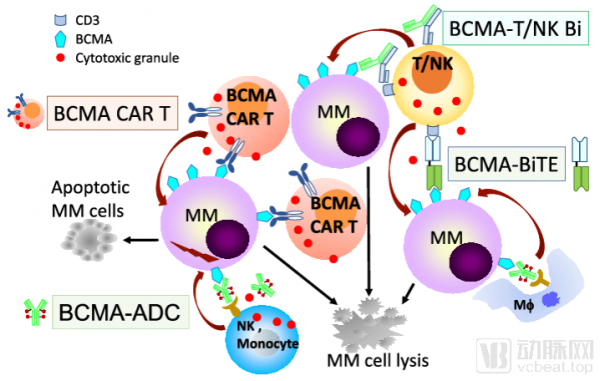
数据来源:research gate
Mustang Bio公司治疗X连锁严重联合免疫缺陷病的MB-107(基因疗法)
被美国FDA授予再生医学先进疗法认定
公司
Mustang Bio公司治疗X连锁严重联合免疫缺陷病(X-linked severe combined immunodeficiency,X-SCID)的MB-107慢病毒载体基因疗法被美国FDA授予再生医学先进疗法认定(RMAT)
药物机理
MB-107是一种创新的基因疗法,该疗法使用慢病毒载体,在体外将健康的IL2RG基因导入从患者体内获得的造血干细胞中。然后将这些经过基因工程改造的造血干细胞注回患者体内
入组标准与实验设计
1/2期临床试验,8名患有X-SCID的婴儿进行了基因治疗
结果
患者不仅恢复了NK细胞和B细胞功能,还有4名婴儿停止了静脉注射免疫球蛋白来提高免疫力。在这4个婴儿中有3个婴儿对疫苗产生了抗体反应,这也证实了其B细胞功能性
美国FDA接受了安斯泰来提交的Xtandi的补充新药申请,
治疗转移性激素敏感性前列腺癌(mHSPC)患者
公司
安斯泰来和辉瑞公司宣布,美国FDA接受了为Xtandi(enzalutamide)递交的补充新药申请(sNDA),治疗转移性激素敏感性前列腺癌(mHSPC)患者
药物机理
Xtandi是一种特异性雄激素受体抑制剂,它不但能够阻断雄激素与受体的结合,而且能够抑制受体向细胞核内转移,且抑制雄激素受体与DNA的结合
入组标准与实验设计
在随机双盲3期临床试验中,1150名mHSPC患者接受了Xtandi或安慰剂的治疗。患者同时接受雄激素剥夺疗法(ADT)
结果
与安慰剂和ADT联用相比,治疗组将患者出现放射学进展或死亡的风险降低61%(HR=0.39, 95% CI:0.30-0.50,p<0.001)
ViiV Healthcare宣布其长效创新HIV双药组合疗法,
在3期临床试验中达到主要终点
公司
ViiV Healthcare公司宣布,长效创新HIV双药组合疗法,在一项名为ATLAS-2M的3期临床试验中达到主要终点。
药物机理
在双药组合中,Rilpivirine是已经在美国和欧盟获批的口服非核苷逆转录酶抑制剂(NNRTI),而cabotegravir为正在开发阶段的整合酶抑制剂(INI)
入组标准与实验设计
在为期48周的随机、开放标签、含活性对照研究中,1045名感染HIV-1病毒的患者,每8周注射一次和每4周注射一次,进行疗效对比
结果
每8周注射一次后的总体安全性和抗病毒活性与每4周注射一次方案的结果一致
美国FDA接受百济神州为BTK抑制剂泽布替尼递交的新药申请,
用于治疗复发/难治性套细胞淋巴瘤(R/R MCL)
公司
百济神州宣布,美国FDA已经接受该公司为BTK抑制剂泽布替尼(zanubrutinib)递交的新药申请,用于治疗复发/难治性套细胞淋巴瘤(R/R MCL)患者。同时,FDA授予这一新药申请优先审评资格
药物机理
泽布替尼(zanubrutinib)为一款BTK抑制剂
入组标准与实验设计
实验包括1项B细胞淋巴瘤患者的全球性1/2期临床,一项在中国开展的治疗R/R MCL患者的多中心2期临床,以及在包括641名患者的5项临床试验中获得的安全数据和非临床数据
结果
在中国的关键性2期中,总缓解率(ORR )达到83.5%,完全缓解率为58.8%,部分缓解率(PR)为24.7%。在全球性1/2期临床中,ORR为85.4%,CR为29.2%,PR为56.3%
Eiger BioPharmaceuticals开发的聚乙二醇化干扰素λ获得突破性疗法认定,
治疗丁肝病毒(HDV)感染
公司
专注于研发罕见病靶向治疗的Eiger BioPharmaceuticals公司宣布,该公司开发的聚乙二醇化干扰素λ(Lambda)获得FDA授予的突破性疗法认定,治疗丁肝病毒(HDV)感染。
药物机理
Lambda是“first-in-class”III型干扰素(type III IFN),能在病毒感染期间刺激免疫应答,达到保护宿主的目的
入组标准与实验设计
在2期临床试验LIMT(Lambda Interferon Mono Therapy)中,33例HDV感染患者接受了治疗
结果
在接受治疗24周之后,患者的持久病毒学缓解率(durable virologic response)达到36%。这一数值优于历史上聚乙二醇化IFNα的表现
Cassiopea公司向FDA递交了局部雄激素受体抑制剂
clascoterone 1%霜剂的新药申请,用于治疗痤疮
公司
专注于开发新机制皮肤病疗法的Cassiopea公司宣布,已为其“first-in-class”局部雄激素受体抑制剂clascoterone 1%霜剂,向FDA递交了新药申请(NDA),用于治疗痤疮
药物机理
Clascoterone旨在成为一款没有全身性副作用,有效和安全的局部雄激素受体抑制剂,用于治疗痤疮或雄激素性脱发
入组标准与实验设计
clascoterone进行了两项关键性3期临床试验
结果
在第52周,分别有57%和62%的试验对象达到研究者整体评分(IGA)两分以上的改善,实现皮肤症状清除(0分)或基本清除(1分)。此外,clascoterone也展示了良好的安全性和耐受性
阿斯利康SGLT2抑制剂达格列净,
在名为DAPA-HF的3期临床试验中达到主要复合终点
公司
阿斯利康(AstraZeneca)公司宣布,该公司的SGLT2抑制剂达格列净(dapagliflozin,商品名Farxiga),在名为DAPA-HF的3期临床试验中达到主要复合终点
药物机理
达格列净是一款“first-in-class”口服SGLT2抑制剂。它已经获得FDA批准,与饮食和锻炼一起,改善2型糖尿病患者的血糖控制
入组标准与实验设计
在3期临床试验中,患者为典型的心衰患者,可能患有或不患有2型糖尿病。射血分数下降心衰患者在接受标准疗法以外,接受达格列净或者安慰剂的治疗
结果
实验的主要复合终点为心衰加重事件(定义为住院或者心衰急诊)或心血管死亡。达格列净达到了试验的主要复合终点。这一试验的详细数据将在未来的医学会议上公布
FDA批准Nabriva Therapeutics的创新抗生素Xenleta上市,
治疗社区获得性细菌性肺炎(CABP)的成人患者
公司
Nabriva Therapeutics公司宣布,FDA批准该公司的创新抗生素Xenleta (lefamulin)上市,治疗社区获得性细菌性肺炎(CABP)的成人患者
药物机理
lefamulin是一种创新截短侧耳素(pleuromutilin)类抗生素,通过与细菌核糖体的肽基转移酶中心(PTC)相结合,能够抑制细菌的蛋白合成,从而达到抑制细菌生长的效果
入组标准与实验设计
在二项关键性3期临床试验中,评估了静脉注射和口服lefamulin与莫西沙星相比,治疗成人CABP的安全性和有效性,共计1289名患者参与试验
结果
lefamulin的疗效与莫西沙星相比达到非劣效性(non-inferiority)
卡瑞利珠单抗治疗cHL关键II期数据正式发表:客观缓解率76.0%
公司
恒瑞的PD-1卡瑞利珠单抗治疗至复发或难治性经典型霍奇金淋巴瘤(cHL)患者的2期数据正式公布,客观缓解率76.0%
药物机理
卡瑞利珠单抗是PD1抑制剂
入组标准与实验设计
在关键II期试验中,中国14家中心入组了75例平均年龄34岁(22-77岁)的复发或难治性cHL患者,通过静脉注射给予每2周1次的卡瑞利珠单抗200 mg
结果
32例(42.7%)患者因疾病出现进展停止了卡瑞利珠单抗治疗,其余43例患者仍在接受治疗。ORR为76.0%(57/75),其中完全缓解率28.0%(21/75),部分缓解率48.0%(36/75)
卡瑞利珠单抗的2期结果

数据来源:clinical cancer research
其 他 资 讯
信达生物与Incyte公司联合申报的JAK1抑制剂itacitinib的临床试验申请,获得中国国家药监局药品审评中心(CDE)的受理。目前,中国尚未有对JAK蛋白激酶家族具有选择性的第二代JAK抑制剂上市
Pharming公司宣布与诺华(Novartis)公司达成一项合作协议,根据协议,Pharming公司将获得开发与商品化CDZ173的独家许可。这是诺华公司开发的一种小分子磷脂酰肌醇3-激酶(PI3Kδ)抑制剂,可用于治疗磷脂酰肌醇3-激酶δ综合征(“APDS”)
安进与艾尔建公布了利妥昔单抗生物仿制药ABP798疗效比较研究的积极顶线结果。截至目前,共23款生物仿制药获得批准,有9款针对罗氏三大王牌药,其中Mvasi和Kanjinti已于今年7月中旬在美国市场上市,成为该市场上市的首个安维汀和赫赛汀生物仿制药
与诺华SMA基因疗法Zolgensma相关的数据操纵丑闻正在不断发酵,而这正在损害外界对公司首席执行官Vas Narasimhan的信任。目前为止,诺华已解雇了涉及Zolgensma数据操纵的5名科学家,并任命了新的AveXis公司首席科学官
国家医保局和人力资源社会保障部联合下发《国家基本医疗保险、工伤保险和生育保险药品目录》,本次发布的常规准入部分共2643个药品,包括西药1322个、中成药1321个(含民族药93个)。中药饮片采用准入法管理,共纳入892个。从调出的品种看,共调出150个品种,其中约一半是被国家药监部门撤销文号的药品
-
法无禁止即可为!网售处方药事实上开了“绿灯”!全面解读最新的药品管理法2019-08-27
-
智慧医疗:国产医疗机器人再获世界500 强关注2019-08-27
-
新版药品管理法来了!这些新变化需要知道2019-08-27
-
全面解析新版医保目录对医药全行业的影响(下): 以治疗性药品为主导,中药注射剂无一新增!2019-08-27
-
医疗资本出海:90%投技术流,腾讯投得早、BV百度偏早期,高瓴与通和深耕创新药2019-08-26
-
医疗健康行业上半年500余家机构进场2019-08-26
-
基层医疗机构引入便民“智慧元素”2019-08-26
-
深圳喜迎政策利好:智慧医疗产业下一步该怎么走?2019-08-26
-
可穿戴医疗设备已死?苹果健康团队内乱,行业前景不明!2019-08-23
-
微软将三星电子前首席医疗官David Rhew招致麾下,担任微软全球首席医疗官和医疗保健副总裁2019-08-23
-
西北大学生命愿景与智慧医疗研究院成立2019-08-23
-
4年投入近200亿美元!9起投资6次并购,英特尔强势挺进医疗市场2019-08-23
-
2019世界机器人大会开幕 5G应用助力智慧医疗2019-08-23
-
波士顿科学公司完成对英国医疗设备制造商BTG的收购,增强其介入医疗产品组合2019-08-21
-
郑州5G+智慧医疗加快布局2019-08-21