一波未平一波又起的缬沙坦事件,NMPA、FDA、EMA对亚硝胺杂质如何管理?
一波未平一波又起的缬沙坦事件,NMPA、FDA、EMA对亚硝胺杂质如何管理?2019年9月13日,美国食品药品监督管理局(FDA)发布声明称,一些雷尼替丁药物(包括Zantac等为
2019年9月13日,美国食品药品监督管理局(FDA)发布声明称,一些雷尼替丁药物(包括Zantac等为人熟知的治疗胃溃疡药品)含有一种称为N-亚硝基二甲胺(NDMA)的亚硝胺杂质。同日,欧洲药品管理局(EMA)的执行董事也发表声明,要求人类药物委员会(CHMP)提供指导如何避免人用药物中的亚硝胺的方法,并表示在一家公司的吡格列酮和雷尼替丁样品中检测到亚硝胺杂质。目前,FDA和EMA已经开始在美国和欧盟范围内对雷尼替丁进行审查。
这次在雷尼替丁中发现的杂质NDMA并不让人感到陌生,它正是一年前引发华海缬沙坦巨大风波中的主角。
华海缬沙坦事件回顾
2018年,华海因生产的缬沙坦原料药中发现杂质NDMA,引发EMA和FDA调查。7月5日EMA发布召回公告,表示获知华海川南工厂生产的缬沙坦中检测出NDMA杂质,随机抽检杂质含量为3.4-122 ppm,平均值为66.5ppm。根据ICH(人用药品注册技术要求国际协调会议)指导原则M7为限制潜在致癌风险而对药物中DNA活性(诱变性)杂质进行的评估和控制,认为该杂质水平需引发警惕。FDA则于7月底至8月初对华海川南工厂进行现场检查,9月28日将其列入进口禁令66-40。
根据FDA警告信,笔者梳理出一条华海缬沙坦NDMA问题的时间线,见下表
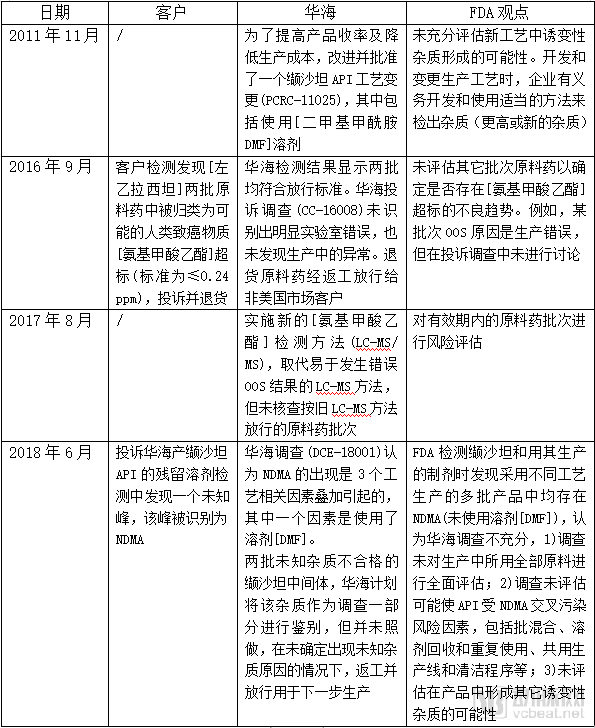
[ ]:FDA警告信中隐藏信息,参考华海药业的翻译文件补齐
华海表示,发现NDMA杂质时,各国监管部门尚未对该杂质制定可接受控制限度的行业标准,其缬沙坦现行工艺分别于2012年、2013年经过了EMA和FDA批准,符合法规标准。
但FDA提醒,通用行业规范可能并不总与CGMP要求保持一致,企业需要对其生产药品质量负责。ICH M7提示,变更原料药生产工艺时,变更评估要确定是否会导致任何新的诱变杂质或已知诱变杂质更高的接受标准。FDA与制造商密切合作,解决产品中的杂质问题,增加紧缺药物供应。
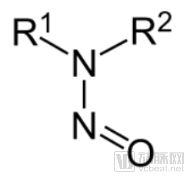
亚硝酸化合物
在2018年6月之前,NDMA和NDEA不在已确定的沙坦类药物杂质中,因此常规测试未检测到。有些沙坦含有一种特殊的环结构(四唑环),在某些条件下,当使用某些溶剂、试剂和原材料时,合成过程中可能生产形成亚硝胺杂质。此外,当制造商在制造过程中使用了受污染的设备或试剂也会导致药物中存在杂质。没有四唑环的其他类药物,如阿齐沙坦、依普罗沙坦和替米沙坦,暂不涉及此风险。
NMDA事件给华海制药带来巨大影响,2017年度,华海药业缬沙坦原料药销售收入为3.28亿元,缬沙坦制剂销售额为2043万美元。2018年美国停止进口华海生产的缬沙坦原料药以及用这些原料药制成的制剂,欧盟也禁止华海药业浙江临海川南工厂产品入境。华海除停产停供带来的直接损失外,还将面临产品召回,客户赔偿以及后续可能发生的诉讼费用。
同时受到震荡的还有超过百亿市值的沙坦类药物市场。华海之后,由于Aurobindo、Mylan、Sandoz、Teva等其他公司成品中也发现了NMDA或NDEA,引发了上千批次缬沙坦、氯沙坦、雷尼替丁的召回,造成关键药物(包括缬沙坦和氯沙坦药品)短缺,迫使FDA加快和优先审查能缓解短缺的新药或仿制药申请。2019年3月,FDA优先审查和批准了印度制药公司Alkem Laboratories Limited的仿制药Diovan(缬沙坦)。FDA评估了该公司的制造工艺,确保他们使用了适当测试方法来证明获批缬沙坦产品不包含NDMA或NDEA,不存在其他亚硝胺杂质形成的已知风险。
各国管理办法
NDMA和NDEA(N-亚硝基二乙胺)都是亚硝胺杂质,经动物试验确定为动物致癌物,目前被列为人类可疑遗传毒性致癌物。EMA引用一篇综述评估了亚硝胺杂质可能导致的最高癌症风险(根据动物研究推断):在10万名患者中,每天以最高剂量服用华海缬沙坦(按杂质平均含量66.5ppm计算),6年后,这些患者中增加了22例可能因NDMA导致的癌症患者;每天以最高剂量服用4年,可能因NDEA导致的癌症患者人数为8名。
2019年1月31日,EMA建议生产沙坦降压药的公司审查其生产工艺,以避免产生亚硝胺杂质,并根据现行国际准则,为NDMA和NDEA设定了过渡期临时限值。通过基于动物研究中每种杂质的最大每日摄入量(NDMA:96.0ng,NDEA:26.5ng),除以每种活性物质的最大日剂量,计算得到限值(见下表)。
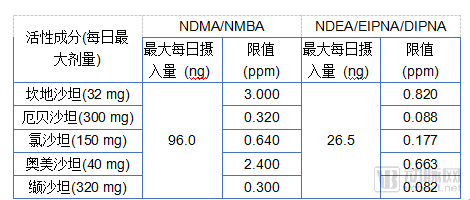
随后,FDA又在某些氯沙坦产品中发现了新亚硝胺杂质,即N-亚硝基-N-甲基-4-氨基丁酸(NMBA)。根据初步评估,暴露于NMBA的患者患癌症的风险增加比例与暴露于NDMA的患者相似,但低于暴露于NDEA的风险。2019年2月28日,FDA发布了血管紧张素Ⅱ受体阻滞剂(ARBs)中NDMA、NDEA和NMBA杂质临时限值(见下表)
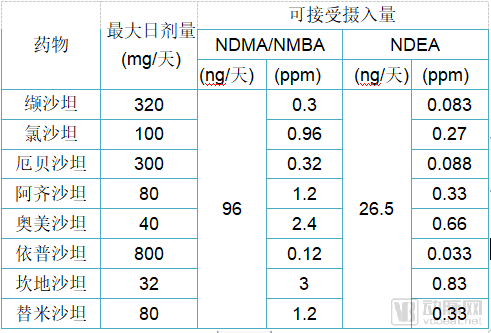
欧洲药品和保健质量管理局(EDQM)网站上可查阅欧盟官方药品检验实验室制定的检测沙坦类药物NDMA和NDEA方法*,并可基于这些方法开发和验证适用于其他API中亚硝胺杂质的分析方法。
EMA于2019年9月19日和26日发布通告要求人用药上市许可持有人(MAH)在6个月内审查其药物中存在的亚硝胺污染风险,如在药物中检测到亚硝胺,则MAH必须及时通知EMA,以便采取适当的监管措施。优先考虑高风险产品,在3年内解决亚硝胺污染问题。FDA也发布了沙坦类和雷尼替丁等药物中亚硝胺杂质的检测方法。
首页 下一页 上一页 尾页-
CeMAT ASIA 2019|仙知机器人完美收官,下一站再见2019-10-28
-
CeMAT Asia 2019 最大“靓”点:人机混场,木蚁打破物流机器人瓶颈2019-10-25
-
CeMAT ASIA 2019,仙知机器人为何会与众不同?2019-10-25
-
迦智科技携智造物流解决方案抢眼CeMAT ASIA 20192019-10-25
-
CeMAT ASIA 2019|仙知机器人强势登场,现场展示打造移动机器人2019-10-23
-
旷视重磅亮相CeMAT ASIA 2019 用河图驱动智慧物流产业生态2019-10-23
-
数字疗法2019的24项突破性进展,超过20款获得FDA认证2019-10-23
-
欧洲药品管理局重视医药领域的技术创新,提出2025年的五大监管目标2019-10-22
-
CeMAT ASIA 2019展前预告|仙知机器人邀您现场体验如何打造移动机器人2019-10-18
-
又一款AI产品获FDA认证!10倍速MRI检验有望在AI支持下实现2019-10-17
-
斯坦德将亮相CeMAT亚洲国际物流展,助力国际物流自动化2019-10-16
-
CeMAT ASIA 2019展会预告|找仙知,打造你的专属移动机器人2019-10-14
-
AI用于疾病诊断和新药品设计的前景可观2019-10-14
-
药品信息化追溯体系正在加码,从0到1的体系建设带来这三大趋势2019-10-12
-
3D Systems的VSP骨科虚拟手术规划平台获得FDA许可2019-09-29